5.ヒドロホウ素化-酸化 これは先ほど紹介した オキシ水銀化-脱水銀化 とは 逆のことをしたい時の反応だ。 つまり大きな目的としては OH1個を 置換基が少ない アルケンのCにつけたい時に使われるってことだね。 では例を見ていこう。テトラヒドロフラン(thf) やジメチルスル フィドとの錯体は還元力が強いのでカルボン酸などの還元、ヒドロホ ウ素化反応に用いる。 • シアノトリヒドロホウ酸ナトリウム(nabh 3 cn) 水素化ホウ素ナトリウムよりも還元力は低いが、酸性の水中での不活性ガス充填 避けるべき条件 湿気(分解) CAS RN Reaxys Registry Number PubChem Substance ID

ホウ素化 Wikiwand
ヒドロホウ素化 加水分解 反応機構
ヒドロホウ素化 加水分解 反応機構-アルケンのヒドロホウ素化-酸化反応でアルコールを得る。 c ch2 h3c h3c c ch3 h3c ch2oh h 1) bh3/ether 2) h2o2/oh/h2o (5)カルボン酸エステルの加水分解:ヒドロホウ素化-酸化とはどういう反応か ch3chch2 ch3chch2 hb hh bh3 ch3chch2 hb –oh, h 2o2, h2o ch3chch2 hoh 2つの異なる反応を続けて行う ① アルケンのヒドロホウ素化 ② アルキルボランの酸化 アルキルボラン アルコール ※ ここに「h」を書いてないのは、アルケンが
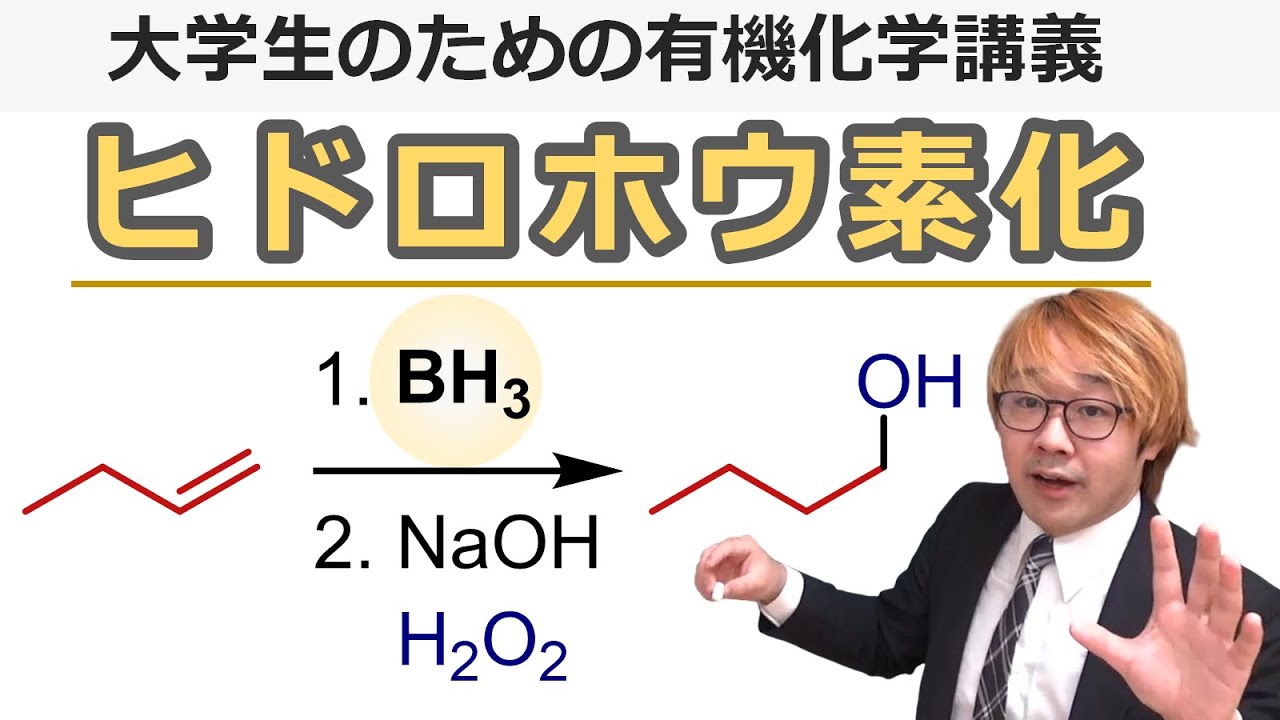



大学有機化学 ヒドロホウ素化の反応機構と反応条件 アンチマルコフニコフ則のアルコール合成法 Youtube
水と反応して水素を発生しながら,硼 酸とピナコール になる。空気中の酸素,二 酸化炭素,湿 気と反応。 3 用 途 31 アルキンのヒドロホウ素化反応 pinbは,bh3錯 体に比べて還元力が弱いので,ヒ ド ロホウ素化反応の試薬としての汎用性が高い。例えばクそれが『有機化学 基本の反応機構(日本語/英語版)』です! 本アプリには電子の流れを表す「巻矢印」を用いて反応機構を詳しく説明した動画が106個も含まれており、大学の1〜2年時の有機化学の基礎知識の習得に役立ちます。 一度ダウンロードすればそれが『有機化学 基本の反応機構(日本語/英語版)』です! 本アプリには電子の流れを表す「巻矢印」を用いて反応機構を詳しく説明した動画が106個も含まれており、大学の1〜2年時の有機化学の基礎知識の習得に役立ちます。 一度ダウンロードすれば
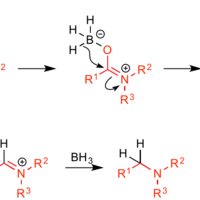
ヒドロホウ素化(ヒドロホウそか)あるいはホウ水素化(ホウすいそか)、ハイドロボレーション (hydroboration) は1956年にハーバート・ブラウンらによって報告された化学反応で、ボランがアルケンまたはアルキンに付加する反応である。 この反応の開発によりブラウンは1979年のノーベル化学賞ホウ素化を含む多くの新規ボリル化反 応の開発に取り組んできた3)。今後よ り重要性を増すと思われるのは、ボロ ニル基を保持したまま行う有機ボロン 酸の官能基化反応である。もちろんボ ロニル基自身やそのエステル体は一定 の反応条件では失われるLeuckart反応3)やEschweilerClarke反応4)が知られており, ギ酸F0513が還元剤として用いられていました。現在では シアノ水素化ホウ素ナトリウムS0396が用いられることが 多くなり,Borch反応 5)として知られるようになりました が,S0396は毒性が強いという問題点
などの多価フェノールとホウ酸またはハロゲン化ホウ素 との反応でできる7)。これらは容易に加水分解して しま 〓うことが実用に応用される場合問題になる。このような ホウ素高分子化合物はケイ素高分子化合物の後を追ってヒドロホウ素化−酸化反応 問題2問題1でヒドロホウ素化の際に逆マルコフニコフ則で進行する理由を記せ。 理由① 4中心遷移状態において3級のδの安定性により置換基の少ない方へホウ素が配位する・ヒドロホウ素化 プロペンのように末端に二重結合をもつアルケンをthfとbh 3 で反応させ最初の反応はオレフィンに対するヒドロホウ素化です。 9BBNを用いた一般的な条件が用いられています。 その後、シリカゲル(SiO 2)に吸着させたFeCl 3 を用いたアセタールの加水分解反応により、ケトンを脱保護しています。 その後、ヒドロホウ素化で生じた



2
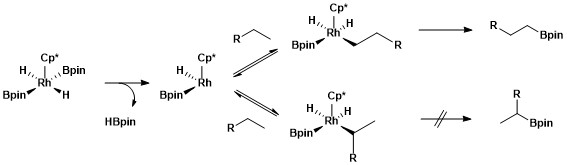



ホウ素化 Wikipedia
ブラウンヒドロホウ素化とは? ノーベル賞受賞者のHCブラウンによって開発されたアルケンをホウ素化する反応です。 得られたアルキルボランは酸化することによって、アルコールに変換することができます。 酸化条件は過酸化水素と塩基をよく用い化学 水素化ホウ素ナトリウムによるアルケンの還元(溶媒dmf)の機構がわかりません。 ボランのヒドロホウ素化と同じような機構かなとも思ったのですが。。。教えてください。9−6 ヒドロホウ素化ー酸化反応 9−7 接触水素化 ハロヒドリンの生成機構 br br δ • アルケンと過酸の反応 • エポキシドの加水分解 r o ooh r o oh o o h2o h3o or ohoh oh oh oh トランスー1,2ージオール 過酸 エポキシド




号 治療指数が改善されたアンフォテリシンb誘導体 Astamuse




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ
SBHは加水分解することで貯蔵エネルギーが倍増し極めて高い効率を示す。 右辺の水素を生成します。 この反応によりボロハイドライドに貯蔵された水素2分子と,水から 2分子の合計4分子の水素を作り出すことになります。 結合力が強いNaBO2に変化する際4623 アルケンのヒドロホウ素化 a ヒドロホウ素化の反応機構 • アルケンにジボラン(ボラン)を反応させると、 付加反応が進行する。 このときの位置選択性は、立体障害と電気陰 性度から逆Markovnikov則に従う。 4623 アルケンのヒドロホウ素化 bアルケンの反応 オキシ水銀化 ヒドロホウ素化 教科書p 545p ~553
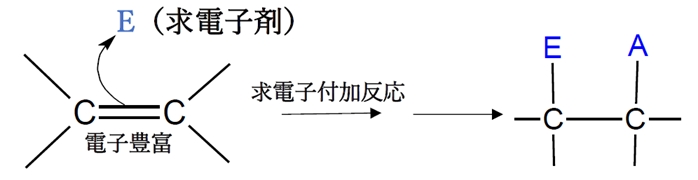



アルケン ヒドロホウ素化 酸化による水和でアルコール生成 回問8c




カルボニル還元 ヒドリド還元とnabh4 Lialh4の反応機構 リョースケ大学
アルケン 過酸反応後酸触媒加水分解とoso4反応後nahso3水処理 106回問103 ルケンからアルコール合成 ヒドロホウ素化-酸化と酸触媒水和の違い 105回問102 ルケン 過酸 エポキシ化 加水分解でエポキシド開環 酸性と塩基性での違い 103回問102化学 有機化学の課題で、ヒドロホウ素化についての問題が出ました。ヒドロホウ素化で生じたアルキルボランを、過酸化水素で酸化する代わりにch3coodで処理するとどうなるか、という問題が出ました。 アOカルボニル化合物の水素化試薬による還元。 oアルデヒドやケトンとGrignard試薬との反応。 oアルケンの水和。 oアルケンのヒドロホウ素化。 oハロゲン化アルキルの加水分解。 o発酵による方法。 ここでは、Ptアルケンの水和"について検討した。
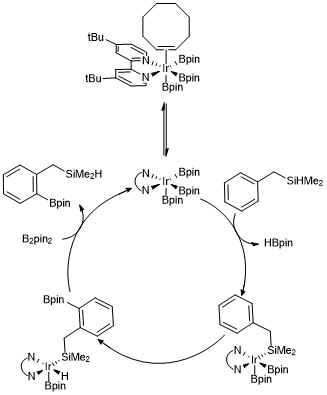



ホウ素化 Wikipedia



ヒドロホウ素化 酸化反応はanti Markovnikov型で進行する水和反応 とらおの有機化学
S152 ヒドロホウ素化における アルキルボランの酸化の反応機構 アルカリ条件におけるアルキルボランの酸化は,hoo–のbへの求核攻撃,ア ルキル基のbからoへの1,2–移動(21章参照),加水分解の順ヒドロホウ素化(ヒドロホウそか)あるいはホウ水素化(ホウすいそか)、ハイドロボレーション (hydroboration) は1956年にハーバート・ブラウンらによって報告された化学反応で、ボランがアルケン又はアルキンに付加する反応である。 この反応の開発によりブラウンは1979年のノーベル化学賞を2オキシ水銀化反応(オキシマーキュレーション) 3ヒドロホウ素化反応(ハイドロボレーション) 4HBrのラジカル付加 5ハロゲン化水素HX の付加 (X=Cl, Br, I) 6ハロゲンX2 の付加(Ⅹ=Cl,Br) 7ハロヒドリンとエポキシドの合成 8過酸によるエポキシド の合成




大学有機化学 ヒドロホウ素化の反応機構と反応条件 アンチマルコフニコフ則のアルコール合成法 Youtube




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ
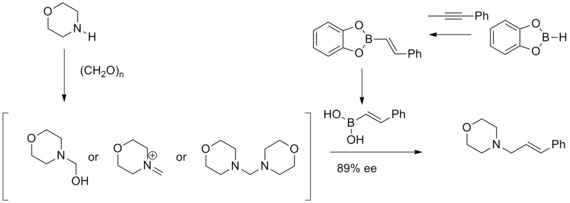
ヒドロホウ素化(ヒドロホウそか)あるいはホウ水素化(ホウすいそか)、ハイドロボレーション (hydroboration) は1956年にハーバート・ブラウンらによって報告された化学反応で、ボランがアルケンまたはアルキンに付加する反応である。 この反応の開発によりブラウンは1979年のノーベル化学賞トランス選択的なヒドロホウ素化反応6Cp*Ru(MeCN)3PF6(Cp*=η5C5Me5) を触媒として用いると、内部アルキンへのヒドロホウ素化がトランス選択的に進行する。 インドールの触媒的不斉ヒドロホウ素化反応7: 脱芳香族化を伴う不斉ヒドロホウ素化反応。ヒドロホウ素化とは、ボラン(BH3)がアルケン(またはアルキン)に付加する反応のことである。 ヒドロホウ素化(ボランのアルケンへの付加)の特徴は、以下がある。 ボランは立体障害が小さい炭素へ結合する(立体特異的) syn付加する(ともに同じほうから付加する) 逆マルコフ



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク



2k基礎有機 章末問題こたえ
Hydroboration と呼ぶ。ヒドロホウ素化に続いて酸化を行う反応は、非対称のアルケン から、水素原子が多く結合している炭素原子に OH 基を導入する方法として知られて いる。この位置選択性は、アルケンに対する水の付加と逆である。酸化ほう素は水と反応してほう酸を生成する際に発熱する19)。 過ほう酸ナトリウムは、室温で加水分解し、分解生成物のメタほう酸ナトリウムと過酸化 水素とは平衡状態にある。メタほう酸ナトリウムは、環境中の温度やpH でほう酸となる)。化反応の機構を示せ. (c) 化合物Bをヒドロホウ素化-酸化すると,シス縮環したデカリン–1–オール誘 導体Cが得られる.ヒドロホウ素化がシン付加で起こる(15章参照)ことを 考慮してCの立体構造を示し,デカリンがシス縮環した構造になる理由をヒ
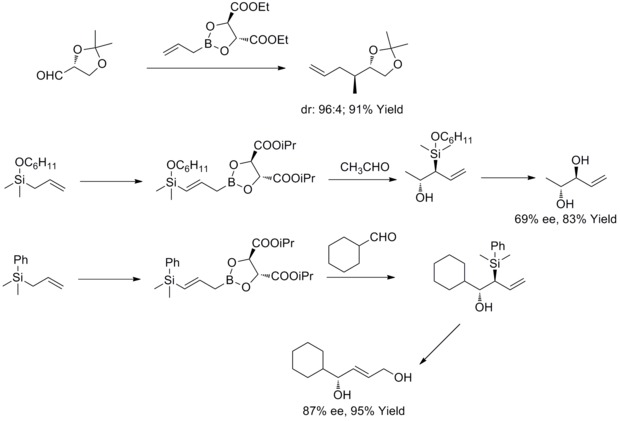



ホウ素化 Wikipedia




ヒドロホウ素化反応 ヒドロホウ素化について質問です 画像を載せまし 化学 教えて Goo



2



1




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ




三成分連結反応のstrecker反応でアミノ酸合成 とらおの有機化学



102 101 105 解説一覧 問101 次の反応のうち 主生成物がラセミ体として生じるのはどれか 1つ選べ Thf テトラヒドロフラン 1はアルケンからアルコールを合成する ヒドロホウ素化 酸化法 で 有名反応のひとつです この反応の特徴は



化学のヒドロホウ素化酸化反応で 生成物の書き方について質問があります 画像 Yahoo 知恵袋




有機化学 基本の反応機構 Organic Chemistry をapp Storeで
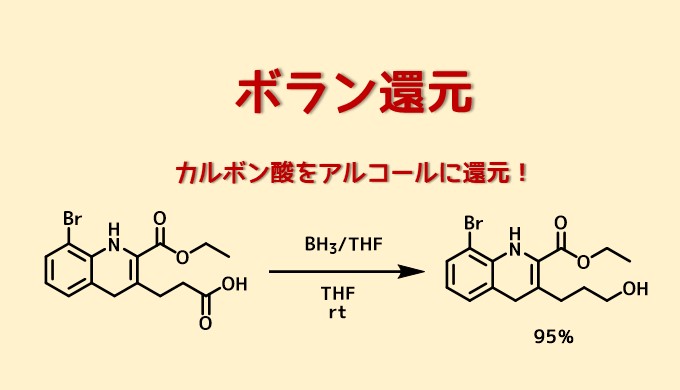



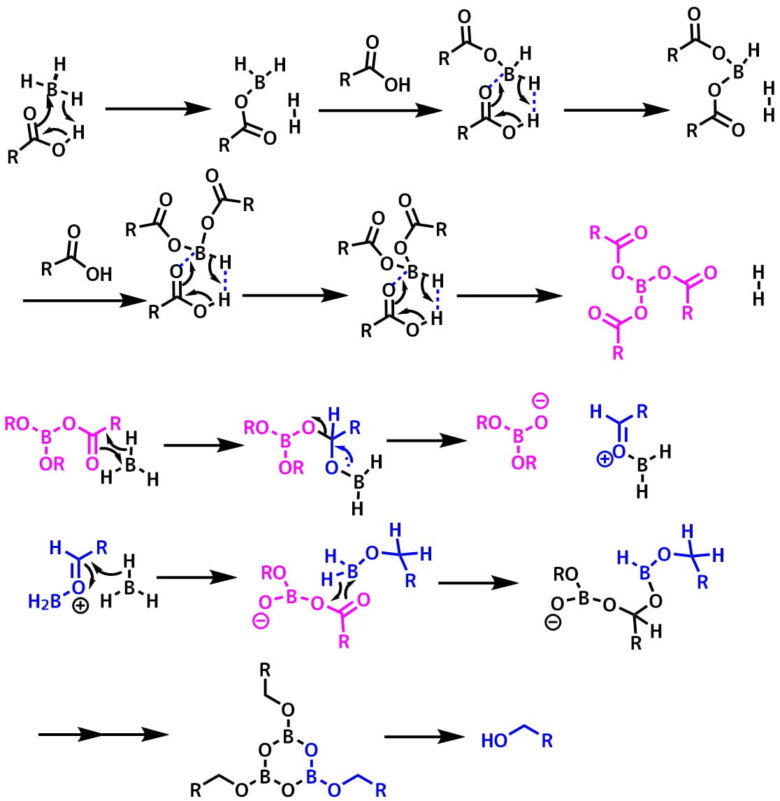
ボラン還元 カルボン酸をアルコールに還元 ネットdeカガク




有機ホウ素化合物の反応 Wikiwand




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ



ホウ素化 Wikipedia



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク



2




ホウ素化 Wikiwand



有機化学 基本の反応機構 Organic Chemistry 日本語 英語 New التطبيقات على Google Play




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ



2k基礎有機 章末問題こたえ




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ



102 101 105 解説一覧 問101 次の反応のうち 主生成物がラセミ体として生じるのはどれか 1つ選べ Thf テトラヒドロフラン 1はアルケンからアルコールを合成する ヒドロホウ素化 酸化法 で 有名反応のひとつです この反応の特徴は



2k基礎有機 章末問題こたえ



ホウ素化 Wikipedia




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ



ボラン還元 カルボン酸をアルコールに還元 ネットdeカガク




ヒドロホウ素化 酸化反応はanti Markovnikov型で進行する水和反応 とらおの有機化学
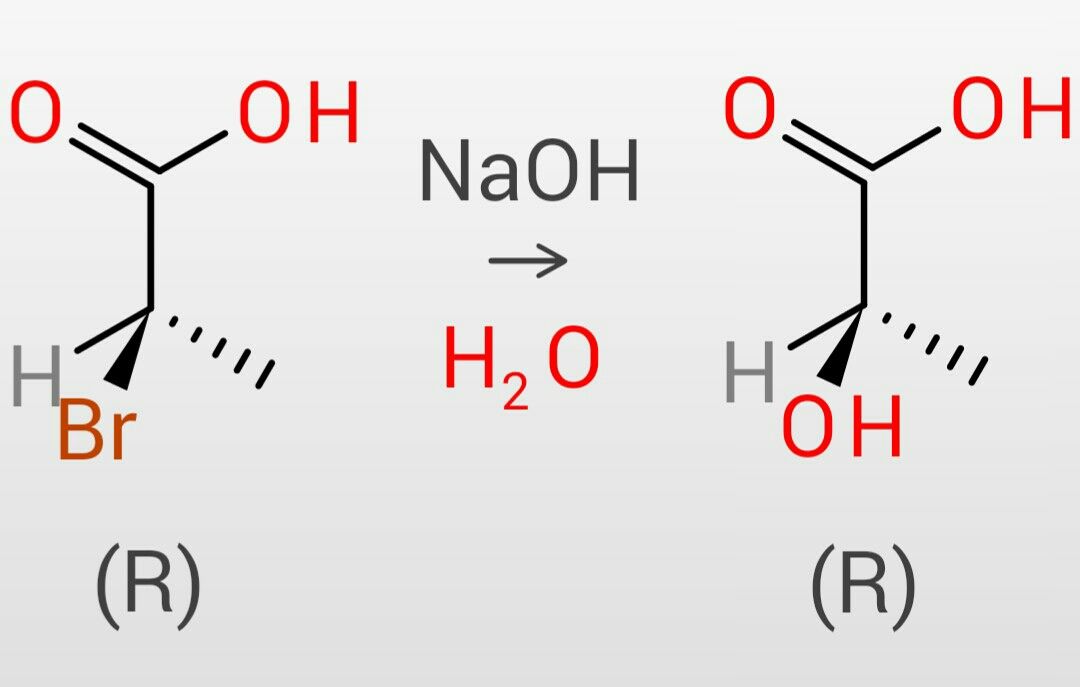



July 16 この世を科学的に知ろう
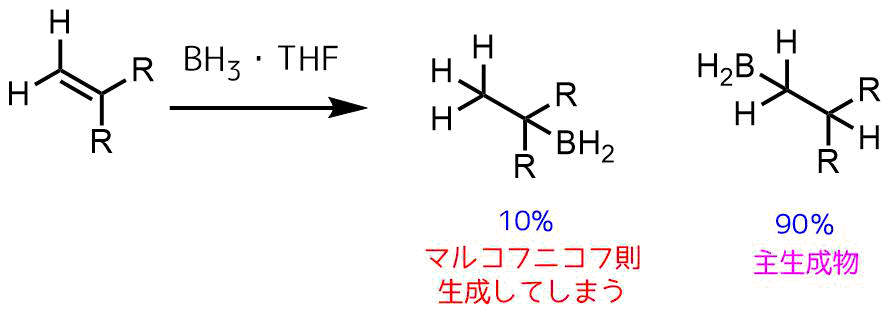



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク
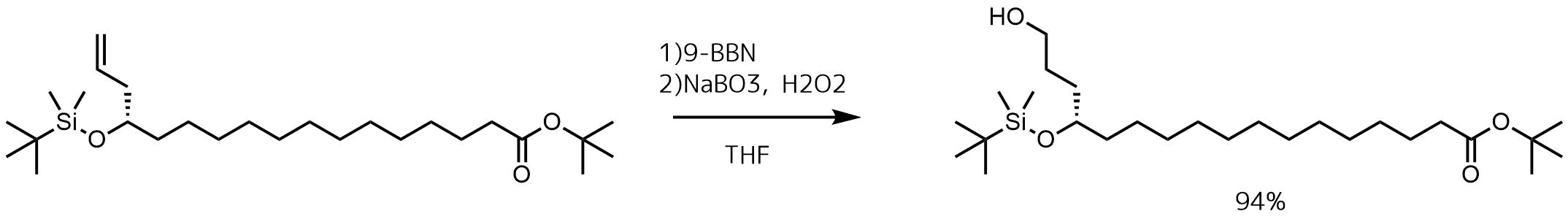



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク




アルケンの反応 猫でもわかる有機化学




某大学様の有機化学学習アプリを開発させていただきました Part2 Awesome Com



2



有機化学 基本の反応機構 Organic Chemistry 日本語 英語 New التطبيقات على Google Play
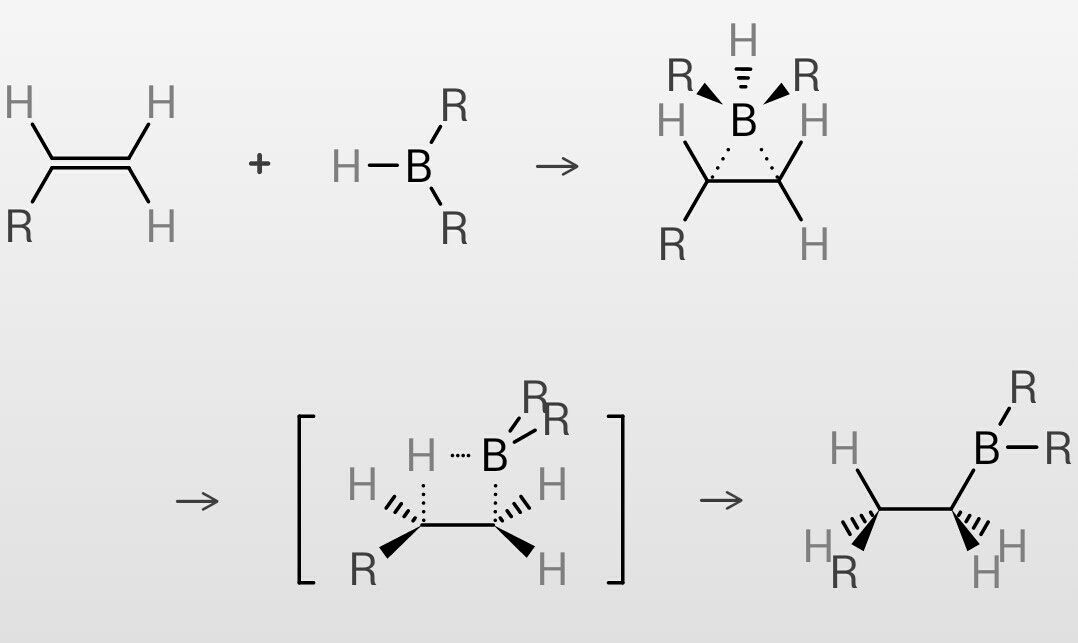



ヒドロホウ素化反応 この世を科学的に知ろう




アルケンの反応 猫でもわかる有機化学



有機化学 基本の反応機構 Organic Chemistry 日本語 英語 Android10以下用 برنامه ها در Google Play




全合成で学ぶ有機化学問題演習1 Shizukaol E 有機化学の扉 Chemorgchem Com




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ
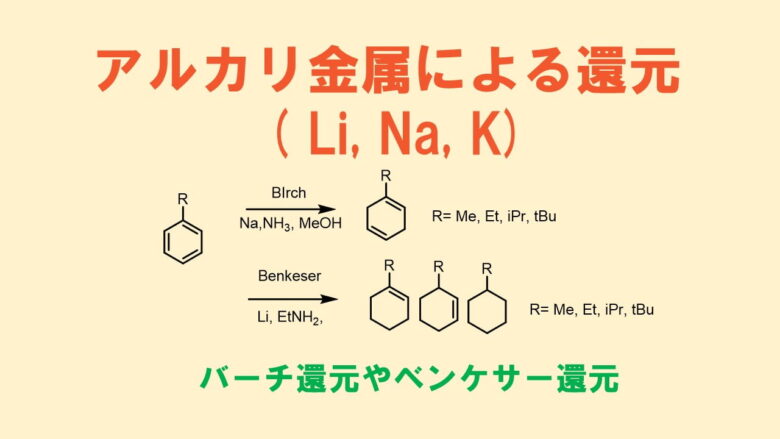



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ




ホウ素化 Wikiwand
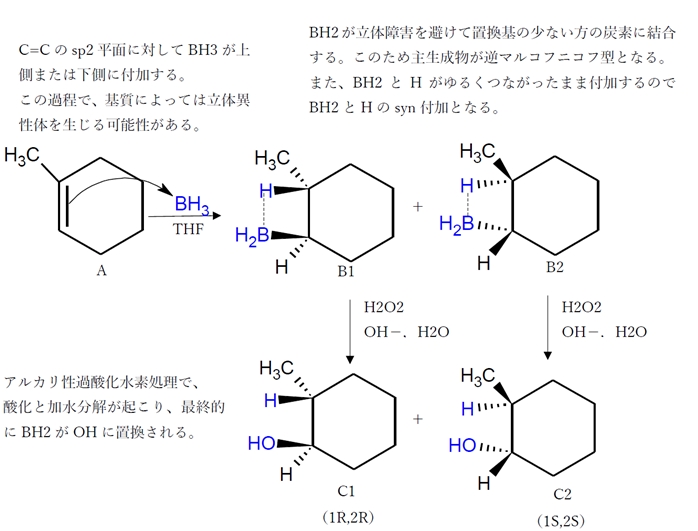



アルケン アルコール合成 ヒドロホウ素化 酸化と酸触媒水和の違い 105回




アルケンの反応 猫でもわかる有機化学




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ
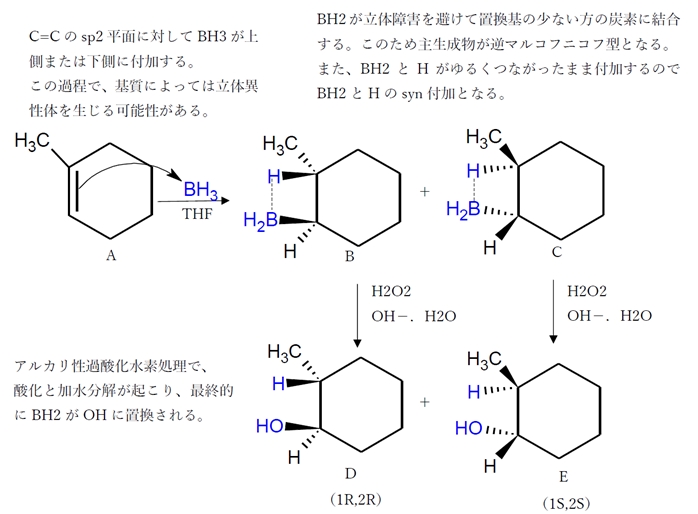



アルケン ヒドロホウ素化 酸化による水和でアルコール生成 回問8c
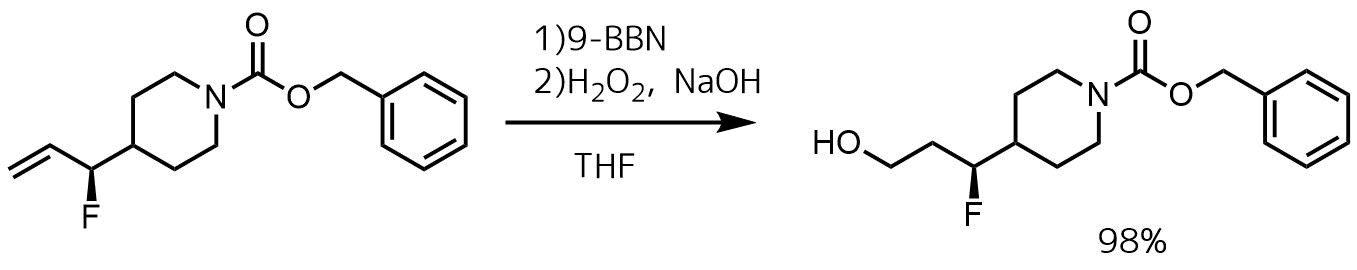



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク
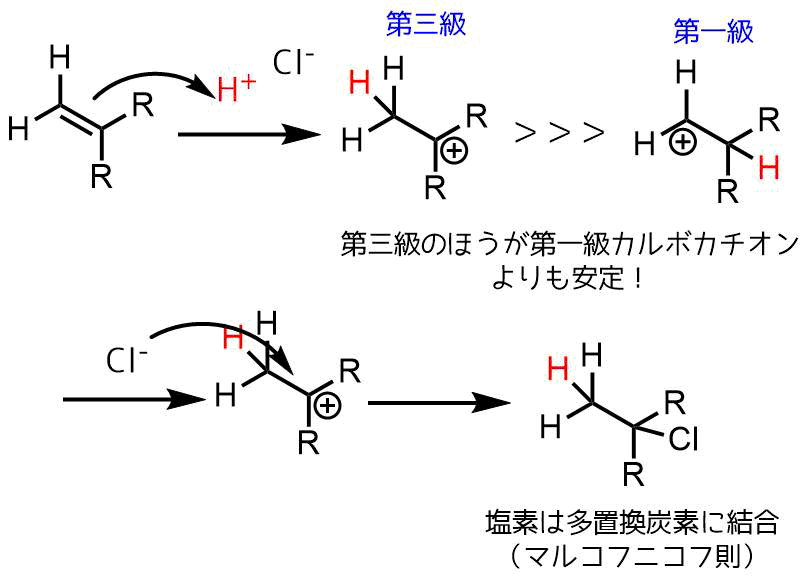



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク




名城大学理工学部応用化学科 永田研究室 有機化学演習 第13回疑問点など




Fischerのエステル化 アプリ 有機化学 基本の反応機構 より Youtube



102 101 105 解説一覧 問101 次の反応のうち 主生成物がラセミ体として生じるのはどれか 1つ選べ Thf テトラヒドロフラン 1はアルケンからアルコールを合成する ヒドロホウ素化 酸化法 で 有名反応のひとつです この反応の特徴は
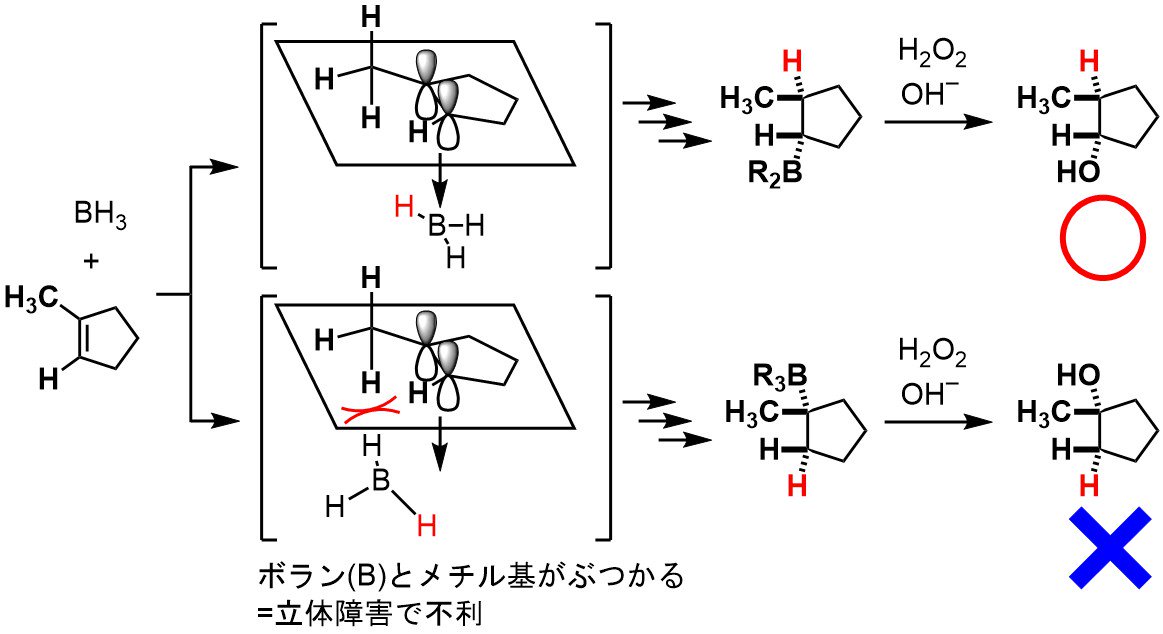



薬学マン ヒドロホウ素化 ヒドロホウ素化 ボラン Bh3 がアルケンに付加する反応 特徴 ボランは立体障害が小さい炭素へ結合する 立体特異的 逆マルコフニコフ則に従う Syn付加する ともに同じほうから付加する 詳細 T Co



Lh3 Googleusercontent Com Proxy 9jp6egotgonvl23ett3h6ucxd9xo1hppsivts0xo6ph Maonqzmopkhhzhafpriml7dofzua40bchp4se Rvxdtbzhbidjjal48afztkv7cv8i7fki8duiuxgbvtuvtlsynvtw6zdu56zwvutxnvgt54 4gt1ehs9ou2tmx7tplepcgefcoan9brgyaiybyxh Ltan0otfwvgkjqelqonpruif8zxq




有機ホウ素化合物の反応 Wikiwand



2




ブラウンヒドロホウ素化 Brown Hydroboration の反応機構 アルケンの水和 Youtube




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ




アルケンの反応 猫でもわかる有機化学



ヒドロホウ素化 酸化反応はanti Markovnikov型で進行する水和反応 とらおの有機化学




ヒドロホウ素化 酸化反応はanti Markovnikov型で進行する水和反応 とらおの有機化学




ホウ素化 Wikipedia
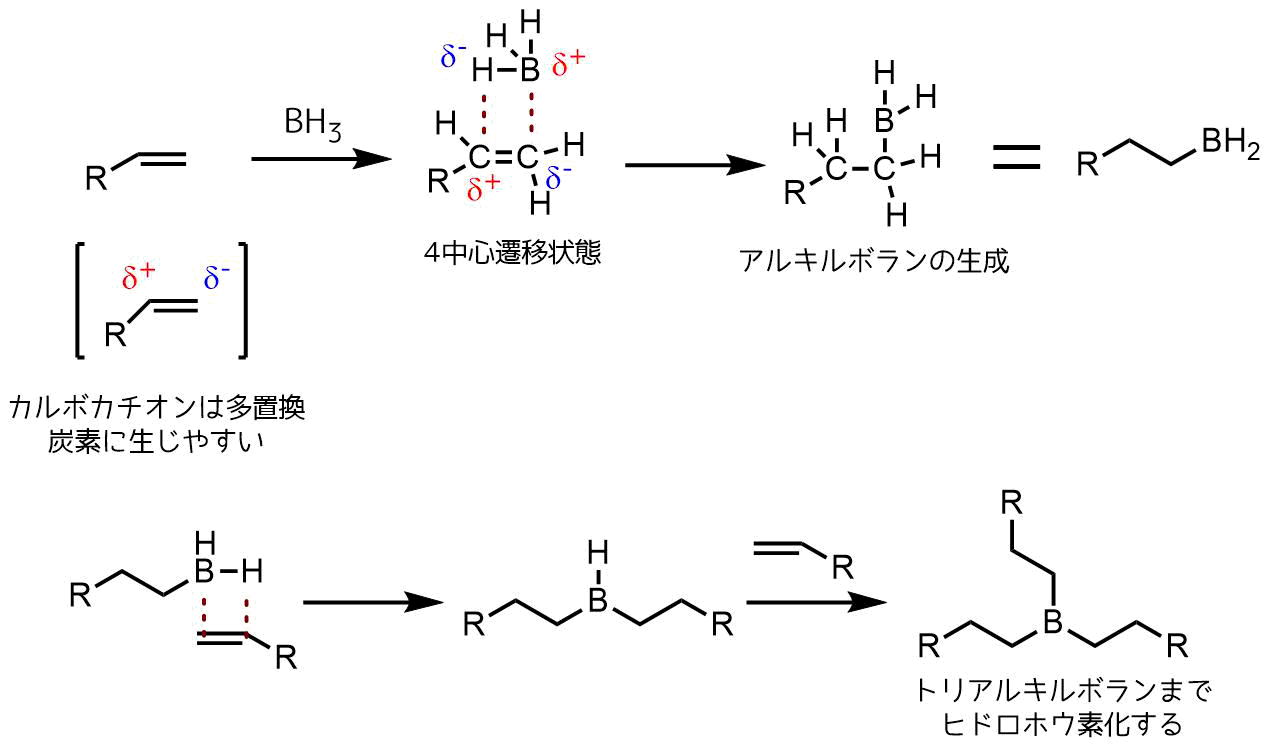



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク



1



4k有機化学 章末問題こたえ



2



2




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ



1



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク



有機化学の反応の主生成物の構造式を求める問題で 質問です 添 Yahoo 知恵袋
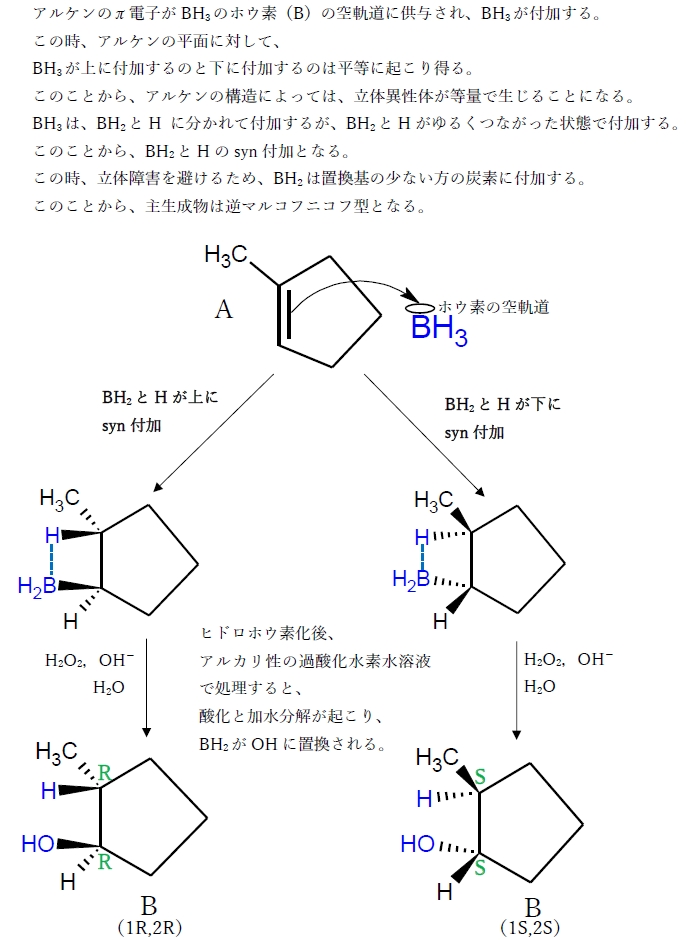



アルケン ヒドロホウ素化 酸化 逆マルコフニコフ シン付加 100回問102




ホウ素化 Wikipedia
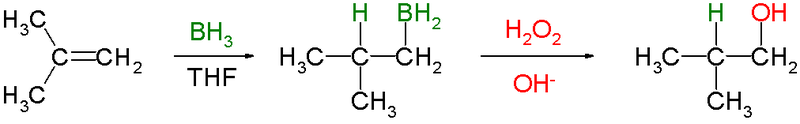



ブラウンヒドロホウ素化反応 アルケンをアルコールに変換 ネットdeカガク




ホウ素化 Wikiwand



ヒドロホウ素化を行うとなぜ逆マルコフニコフが起きるんですか Yahoo 知恵袋




有機化学 基本の反応機構 Organic Chemistry をapp Storeで




ヒドロホウ素化 有機化学勉強会
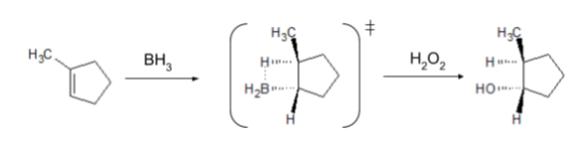



100回薬剤師国家試験 問102解説 薬学 これでok



2k基礎有機 章末問題こたえ




全合成で学ぶ有機化学問題演習1 Shizukaol E 有機化学の扉 Chemorgchem Com
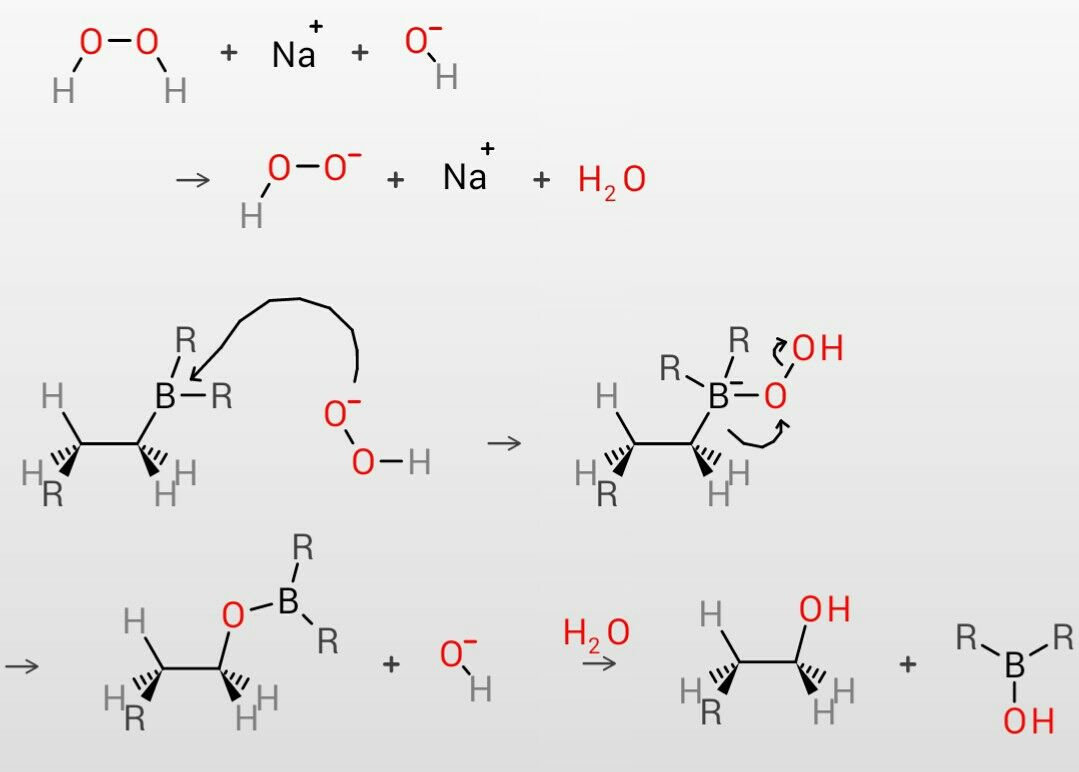



ヒドロホウ素化反応 この世を科学的に知ろう



化学のヒドロホウ素化酸化反応で 生成物の書き方について質問があります 画像 Yahoo 知恵袋




ヒドロホウ素化 酸化反応はanti Markovnikov型で進行する水和反応 とらおの有機化学



2




ブラウンヒドロホウ素化反応 Brown Hydroboration Chem Station ケムステ



102 101 105 解説一覧 Yaku Tik 薬学まとめました




某大学様の有機化学学習アプリを開発させていただきました Awesome Com




全合成で学ぶ有機化学問題演習1 Shizukaol E 有機化学の扉 Chemorgchem Com
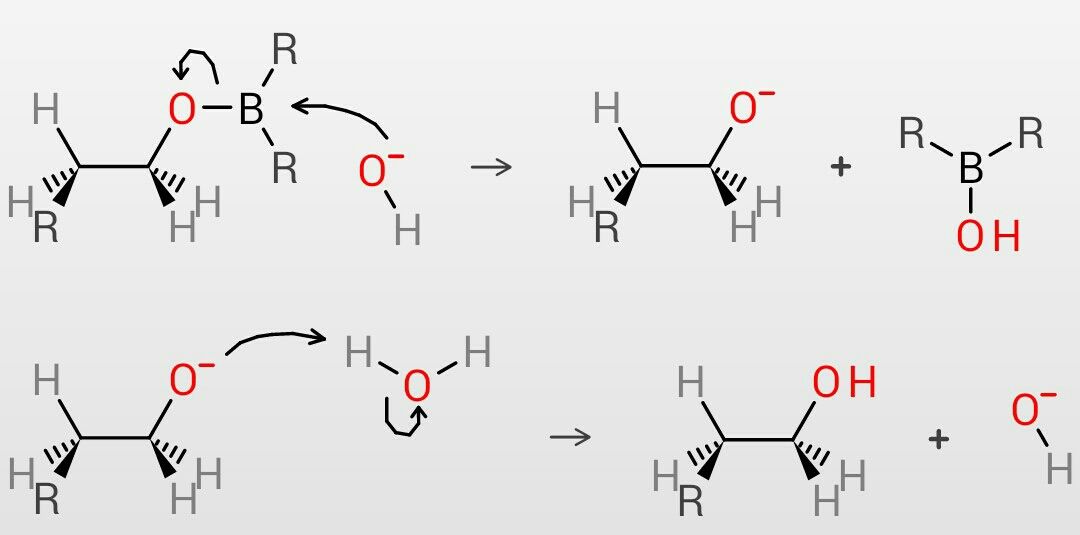



July 12 16 この世を科学的に知ろう



研究内容




有機ホウ素化合物の反応 Wikiwand



1



0 件のコメント:
コメントを投稿